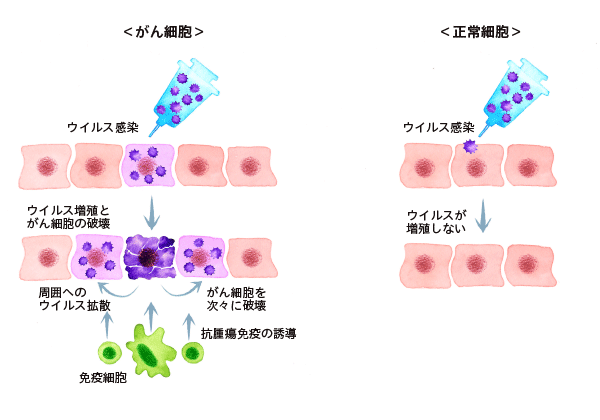
細胞に感染し、細胞を死滅させるウイルス。その仕組みを逆手に取り、がん細胞のみでウイルスが増えて、がん細胞を破壊する治療法が「ウイルス療法」です。ウイルス療法のメカニズムやメリットなどについて、皮膚がんの一種である「
がん細胞のみを攻撃する
人工的なウイルスを薬に
ウイルス療法とは、ウイルスを使ってがんを退治する新しい治療法です。
がん細胞のみで増えるように人工的に改変された遺伝子組み換えウイルスを感染させ、がん細胞を直接破壊します。
この治療に用いられるがん治療用ウイルス「G47
そして2021年6月、がん治療用ウイルスG47
(※1)7年の「期限」内に使用患者全例を対象に検証を行うことを「条件」に承認
藤堂教授らの研究グループの報告(※2)によると、神経膠腫の中でも最も悪性度の高い「
標準的な治療では膠芽腫再発後の1年生存率は平均14%程度といわれ、「ウイルス療法」のがん治療薬による1年生存率はその約6倍になることが示されています。
(※2)「残存・再発膠芽腫への最大6回の腫瘍内反復投与で1年生存率84%―ウイルス療法薬G47
https://www.ims.u-tokyo.ac.jp/imsut/jp/about/press/page_00181.html
がん細胞を破壊し
抗がん免疫を引き起こす
がん治療用ウイルスG47
(※3)日本皮膚科学会 皮膚科Q&A「ヘルペスと帯状疱疹」による
https://www.dermatol.or.jp/qa/qa5/q05.html
単純ヘルペスウイルス1型には、次のような「がん治療に有利な特徴」があります。
- □ヒトの様々な種類の細胞に感染できる
- □細胞を破壊する力が比較的強い
- □抗ウイルス薬が存在するため、必要があれば治療を中断できる
- □患者さんがウイルスに対する抗体を持っていても、治療効果が弱くならない
この単純ヘルペスウイルス1型を人工的に改変したG47
副作用が少ないのもメリット
皮膚がんでも治験
G47
T-hIL12は、G47
悪性黒色腫が治験の対象となった背景には、次のような理由があります。
- □体表面に病変があると、何らかの副作用が生じた場合に見つけて対処しやすい
- □免疫細胞が集まってきやすいがんなので、抗がん免疫刺激機能の効果についても検証しやすい
- □進行のスピードが速いがんなので、その進行や転移を止める効果について結果が早く出やすい
副作用についてはあまり心配がないのではないかという点も、がん治療用ヘルペスウイルスの特徴です。例えばG47
T-hIL12の治験は現在も進行中ですが、現時点では治療後、一時的に発熱が起こる程度にとどまっています。
悪性黒色腫に対する治験によって、T-hIL12が治療薬として承認されれば、さらに食道がん、大腸がん、甲状腺がん、乳がんなど様々ながんへと応用されることが期待できます。
他の治療法との併用で
効果が高まる可能性も
大きな副作用がなく、安全性の高いがんウイルス療法は、がんの3大治療である手術、放射線治療、化学療法(抗がん剤治療)との併用が可能ではないかと言われています。また、悪性黒色腫や
固形がんの治療では通常、「がんを取り除く」ことが治療の第一選択肢となります。ウイルス療法は、手術が不可能な場合や、がんの転移が生じた場合などに、抗がん剤や分子標的薬、免疫チェックポイント阻害薬などと並ぶ選択肢の1つになるでしょう。
さらに、今後臨床応用が進めば、手術の前にがん治療用ヘルペスウイルスを投与して、あらかじめがんを小さくしておく、同時に抗がん免疫を誘導しておく、ということが可能になるかもしれません。そうなると、例えば年々患者数が増加している乳がんなどにおいても、ウイルス療法が手術による体の負担を減らしたり、がんの再発防止につながることも期待できるでしょう。
国内でも複数の企業や大学がすい臓や骨、前立腺、食道などのがんを対象に臨床試験を進めているほか、世界でも研究が行われています。ウイルス療法ががんを制圧する画期的な治療法として一日も早く確立し、多くの患者さんにとって希望の光となることを目指していきます。
信州大学医学部長、臨床研究支援センター・センター長を兼任。日本皮膚科学会・皮膚科専門医。日本臨床薬理学会特別指導医。1989年、東北大学卒業後、同大学皮膚科入局。1995年、東北大学大学院医学系研究科博士課程修了。福島県いわき共立病院皮膚科、米国マサチューセッツ総合病院/ハーバード・メディカルスクールリサーチフェロー、東北大学医学部准教授などを経て、2010年から信州大学医学部皮膚科教授、23年から同大学医学部長に就任、信州大学副学長を兼任。